人類腸道微生物相的發育
發佈日期:2018-11-23
長庚大學教授 林口長庚醫院 婦產部主治醫師 王子豪
2018年10月28的Nature期刊發表了兩篇重要的人類腸道微生物基因體(gut microbiome)論文。Stewart等人代表一個國際合作團隊 (TEDDY, The Environmental Determinants of Diabetes in the Young),從903位三個月到46個月大的嬰兒收集了12,500支糞便檢體,詳細敘述了這些嬰兒腸道微生物基因體的發育變化。該期的Nature封面並將嬰兒的微生物體描述成嬰幼兒的安全防護毯 (security blanket) (下圖),來強調人體和微生物形成一個唇齒相依的密切互利關係。依照嬰幼兒的年紀來分,3個月到14個月大是屬於發育期 (developmental phase),15個月到30個月左右是屬於過渡期 (transitional phase),而大於30個月大則呈現穩定期 (stable phase) (延伸閱讀1)。在人類腸道微生物發育期以比菲德氏菌 (Bifidobacterium) 為主,而在穩定期則以厚壁菌門 (Firmicutes)為主。會影響腸道微生物基因體結構的因素包括:生產的方式(陰道生產或是剖腹產)、是否餵母奶、嬰幼兒是否有兄弟姐妹、或是家裡有是否養毛小孩 (furry pets)當寵物。

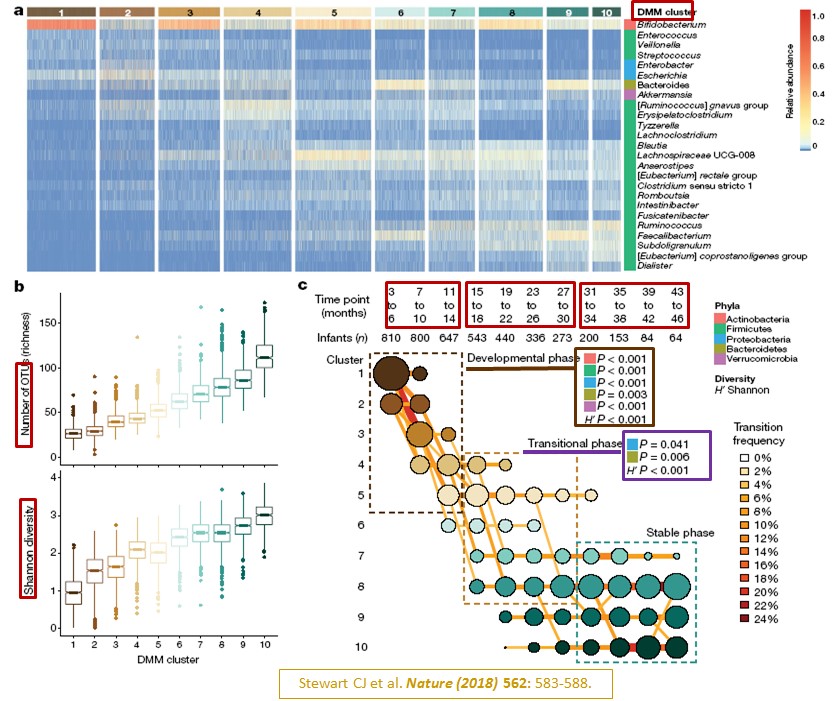
Dirichlet多項混合模型(Dirichlet multinomial mixtures modeling, DMM modeling) 是用來分析微生物總體基因體(microbial metagenomics)資料的概率模型分析法,可以將數據呈現為:在各個檢體中,某一分類單元 (taxa)出現次數的頻率矩陣。該研究利用DMM modeling將排在前25名的主要微生物叢列出,依群聚關係 (clustering)呈現為10個群聚 (clusters),畫出熱度圖 (heat map) (下圖a)。依可操作性分類單元 (OTUs)值和Shannon多樣性指數,進一步分析這十個群聚的同生態域多樣性 (alpha diversity) (見下列註解) (下圖b);而這十個群聚的alpha微生物多樣性,是隨著嬰幼兒的年紀而遞增 (下圖c)。儘管如此,在嬰幼兒的微生物基因體發育期(3個月到14個月大),5個微生物門 (phyla) 的改變會非常顯著 (P < 0.001) (下圖c棕色框); 在嬰幼兒的微生物基因體過渡期(15個月到30個月大) 仍有2個微生物門 (phyla) 的改變非常顯著(下圖c紫色框);而到了微生物基因體的穩定期時,儘管此時期的alpha微生物多樣性最高,但不會再有那幾個微生物門會發生顯著改變了。
(註) 依據DNA序列的相似度來分析,能夠鑒定出微生物的可操作性分類單元 (Operational Taxonomic Units, OTUs)。例如,在一群微生物中根據16S rRNA基因DNA的序列相似度可呈現各種OTUs,而形成的OTUs可能是在細菌的屬或種的層級。Shannon多樣性指數(Shannon’s diversity index)是用來估算群落多樣性高低的指標,例如,當群落中只有一個族群存在時,Shannon指數達最小值0;當群落中有兩個以上的族群存在,且每個族群的個體數量相等時,Shannon指數達到最大值。因為本研究都只有分析腸道(屬同一生態域)的微生物基因體,所以就用這兩個指數 (OTUs和Shannon diversity index)來呈現 Alpha diversity。如果要比較不同生態域 (例如在不同人,或同一人的不同身體部位)所含的微生物多樣性,那就是在描述 Beta diversity (應用於下一篇論文)。
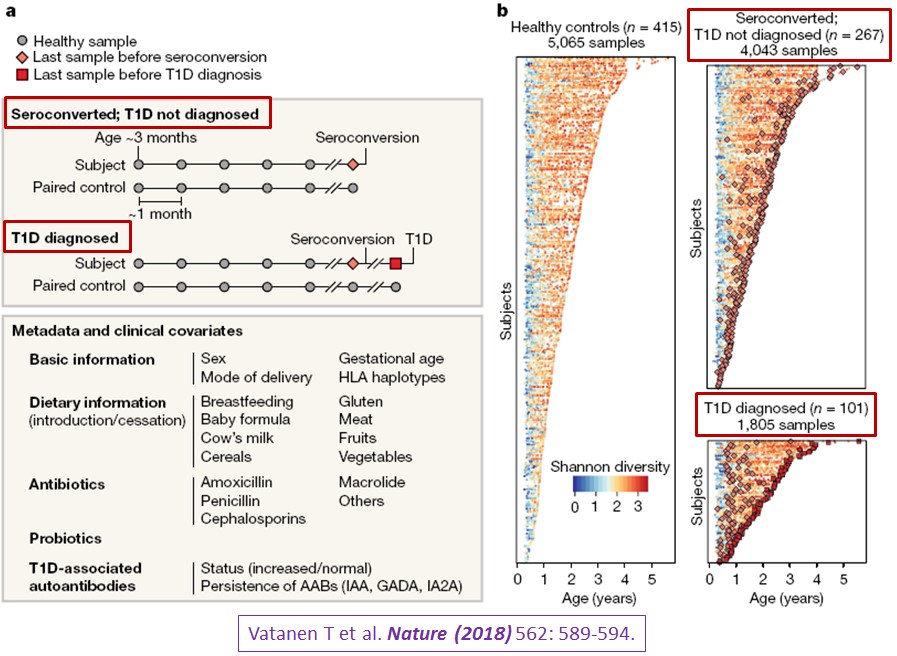
第一型糖尿病是會攻擊胰腺小島貝他細胞 (pancreatic islet beta cells)的自體免疫疾病。第一型糖尿病多是早發的 (early-onset),而和病人的複雜遺傳體質、環境暴露史、和腸道微生物基因體都有相關,尤其病毒感染和嚴重腸道微生物生態失調 (gut dysbiosis)被認為是重要原因。在Vatanen等人為首的國際合作團隊 (也是TEDDY之一) 分析783位白人小孩的10,913糞便檢體的總體基因體學 (延伸閱讀2),其中415位小孩是正常對照組,267位是血清抗體轉換組 (seroconversion, 指已出現對抗胰腺小島的自體免疫抗體 islet autoimmunity但尚未達到第一型糖尿病的診斷),而101位是已確診為第一型糖尿病 (type 1 diabetes, T1D)的病童 (下圖a)。下圖b 則描述三個研究族群中,每一個個案的每次糞便檢體所呈現的Shannon’s alpha diversity:在血清抗體轉換組中每個案的最後檢體(如圖a的菱形符號)就是出現血清抗體轉換的時間點;而在第一型糖尿病族群則依照時間先後而出現菱形符號(血清轉換的時候)和正方形符號(確診為第一型糖尿病的時候)。
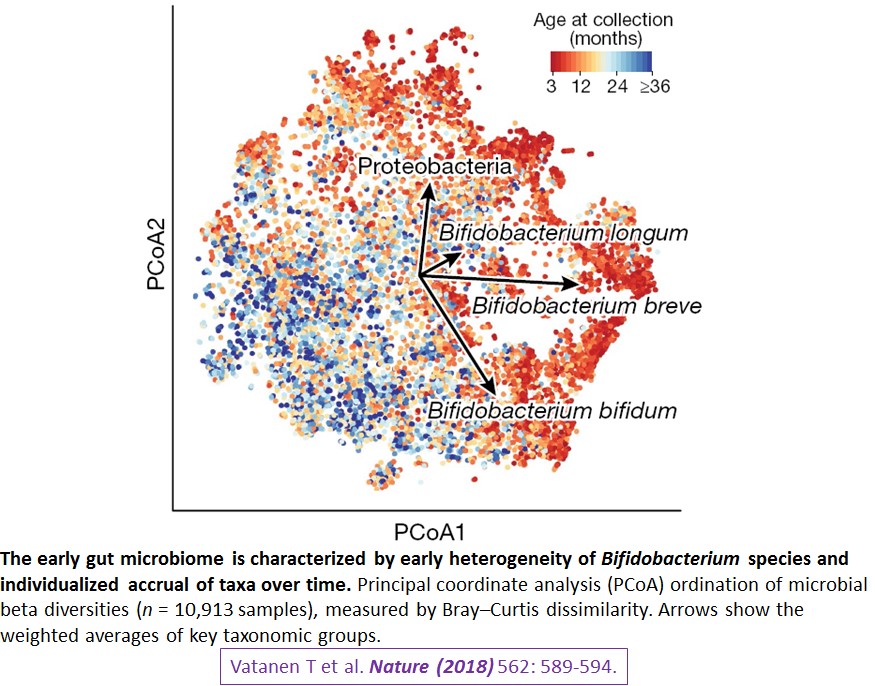
用主要座標分析 (Principal coordinate analysis, PCoA)本研究收到的10,913糞便檢體的微生物,以Bray-Curtis dissimilarity方法依微生物DNA序列來檢定 Beta diversity (如上述:此指在不同人所含的微生物多樣性),可以看到不同嬰幼兒早期的beta微生物多樣性,而這beta微生物多樣性會隨著年紀而逐漸減少 (下圖, 藍色點往左下角移動)。而嬰兒早期的主要腸道微生物是比菲德氏菌 (Bifidobacterium longum, B breve, B bifidum) 和變形菌 (Proteobacteria)。
比較健康對照組和疾病組的腸道微生物差別,發現和血清抗體轉換組比較時,健康對照組有較高的 Lactobacillus rhamnosus,支持早期益生菌補充可保護嬰幼兒不產生對抗胰腺小島的自體免疫抗體 (islet autoimmunity)。而相較於第一型糖尿病人的腸道微生物,健康對照組有較高的 Streptococcus thermophiles和 Lactococcus lactis; 而第一型糖尿病人則含較多的 Bifidobacterium pseudocatenulatum, Roseburia hominis, 和Alistipes shahii。在功能上,健康對照組細菌的綜合發酵能力(fermentation)比較強,能夠增加短鏈脂肪酸 (short chain fatty acids, SCFAs)的產出:包括丁酸類 (butyrate)、乙酸類 (acetate)、和丙酸類 (propionate)。綜合先前許多動物實驗證據,和本研究的人體資料顯示:這些短鏈脂肪酸的產出,有助於減少第一型糖尿病的發生。
延伸閱讀:
- Stewart CJ et al. Temporal development of the gut microbiome in early childhood from the TEDDY study. Nature (2018) 562: 583-588.
- Vatanen T et al. The human gut microbiome in early-onset type 1 diabetes from the TEDDY study. Nature (2018) 562: 589-594.
2018年10月28的Nature期刊發表了兩篇重要的人類腸道微生物基因體(gut microbiome)論文。Stewart等人代表一個國際合作團隊 (TEDDY, The Environmental Determinants of Diabetes in the Young),從903位三個月到46個月大的嬰兒收集了12,500支糞便檢體,詳細敘述了這些嬰兒腸道微生物基因體的發育變化。該期的Nature封面並將嬰兒的微生物體描述成嬰幼兒的安全防護毯 (security blanket) (下圖),來強調人體和微生物形成一個唇齒相依的密切互利關係。依照嬰幼兒的年紀來分,3個月到14個月大是屬於發育期 (developmental phase),15個月到30個月左右是屬於過渡期 (transitional phase),而大於30個月大則呈現穩定期 (stable phase) (延伸閱讀1)。在人類腸道微生物發育期以比菲德氏菌 (Bifidobacterium) 為主,而在穩定期則以厚壁菌門 (Firmicutes)為主。會影響腸道微生物基因體結構的因素包括:生產的方式(陰道生產或是剖腹產)、是否餵母奶、嬰幼兒是否有兄弟姐妹、或是家裡有是否養毛小孩 (furry pets)當寵物。

Dirichlet多項混合模型(Dirichlet multinomial mixtures modeling, DMM modeling) 是用來分析微生物總體基因體(microbial metagenomics)資料的概率模型分析法,可以將數據呈現為:在各個檢體中,某一分類單元 (taxa)出現次數的頻率矩陣。該研究利用DMM modeling將排在前25名的主要微生物叢列出,依群聚關係 (clustering)呈現為10個群聚 (clusters),畫出熱度圖 (heat map) (下圖a)。依可操作性分類單元 (OTUs)值和Shannon多樣性指數,進一步分析這十個群聚的同生態域多樣性 (alpha diversity) (見下列註解) (下圖b);而這十個群聚的alpha微生物多樣性,是隨著嬰幼兒的年紀而遞增 (下圖c)。儘管如此,在嬰幼兒的微生物基因體發育期(3個月到14個月大),5個微生物門 (phyla) 的改變會非常顯著 (P < 0.001) (下圖c棕色框); 在嬰幼兒的微生物基因體過渡期(15個月到30個月大) 仍有2個微生物門 (phyla) 的改變非常顯著(下圖c紫色框);而到了微生物基因體的穩定期時,儘管此時期的alpha微生物多樣性最高,但不會再有那幾個微生物門會發生顯著改變了。

(註) 依據DNA序列的相似度來分析,能夠鑒定出微生物的可操作性分類單元 (Operational Taxonomic Units, OTUs)。例如,在一群微生物中根據16S rRNA基因DNA的序列相似度可呈現各種OTUs,而形成的OTUs可能是在細菌的屬或種的層級。Shannon多樣性指數(Shannon’s diversity index)是用來估算群落多樣性高低的指標,例如,當群落中只有一個族群存在時,Shannon指數達最小值0;當群落中有兩個以上的族群存在,且每個族群的個體數量相等時,Shannon指數達到最大值。因為本研究都只有分析腸道(屬同一生態域)的微生物基因體,所以就用這兩個指數 (OTUs和Shannon diversity index)來呈現 Alpha diversity。如果要比較不同生態域 (例如在不同人,或同一人的不同身體部位)所含的微生物多樣性,那就是在描述 Beta diversity (應用於下一篇論文)。
第一型糖尿病是會攻擊胰腺小島貝他細胞 (pancreatic islet beta cells)的自體免疫疾病。第一型糖尿病多是早發的 (early-onset),而和病人的複雜遺傳體質、環境暴露史、和腸道微生物基因體都有相關,尤其病毒感染和嚴重腸道微生物生態失調 (gut dysbiosis)被認為是重要原因。在Vatanen等人為首的國際合作團隊 (也是TEDDY之一) 分析783位白人小孩的10,913糞便檢體的總體基因體學 (延伸閱讀2),其中415位小孩是正常對照組,267位是血清抗體轉換組 (seroconversion, 指已出現對抗胰腺小島的自體免疫抗體 islet autoimmunity但尚未達到第一型糖尿病的診斷),而101位是已確診為第一型糖尿病 (type 1 diabetes, T1D)的病童 (下圖a)。下圖b 則描述三個研究族群中,每一個個案的每次糞便檢體所呈現的Shannon’s alpha diversity:在血清抗體轉換組中每個案的最後檢體(如圖a的菱形符號)就是出現血清抗體轉換的時間點;而在第一型糖尿病族群則依照時間先後而出現菱形符號(血清轉換的時候)和正方形符號(確診為第一型糖尿病的時候)。

用主要座標分析 (Principal coordinate analysis, PCoA)本研究收到的10,913糞便檢體的微生物,以Bray-Curtis dissimilarity方法依微生物DNA序列來檢定 Beta diversity (如上述:此指在不同人所含的微生物多樣性),可以看到不同嬰幼兒早期的beta微生物多樣性,而這beta微生物多樣性會隨著年紀而逐漸減少 (下圖, 藍色點往左下角移動)。而嬰兒早期的主要腸道微生物是比菲德氏菌 (Bifidobacterium longum, B breve, B bifidum) 和變形菌 (Proteobacteria)。

比較健康對照組和疾病組的腸道微生物差別,發現和血清抗體轉換組比較時,健康對照組有較高的 Lactobacillus rhamnosus,支持早期益生菌補充可保護嬰幼兒不產生對抗胰腺小島的自體免疫抗體 (islet autoimmunity)。而相較於第一型糖尿病人的腸道微生物,健康對照組有較高的 Streptococcus thermophiles和 Lactococcus lactis; 而第一型糖尿病人則含較多的 Bifidobacterium pseudocatenulatum, Roseburia hominis, 和Alistipes shahii。在功能上,健康對照組細菌的綜合發酵能力(fermentation)比較強,能夠增加短鏈脂肪酸 (short chain fatty acids, SCFAs)的產出:包括丁酸類 (butyrate)、乙酸類 (acetate)、和丙酸類 (propionate)。綜合先前許多動物實驗證據,和本研究的人體資料顯示:這些短鏈脂肪酸的產出,有助於減少第一型糖尿病的發生。
延伸閱讀:
- Stewart CJ et al. Temporal development of the gut microbiome in early childhood from the TEDDY study. Nature (2018) 562: 583-588.
- Vatanen T et al. The human gut microbiome in early-onset type 1 diabetes from the TEDDY study. Nature (2018) 562: 589-594.

